BCG: 100 años de la vacuna más antigua aún en uso (y por qué es un «dolor de cabeza» para la ciencia)
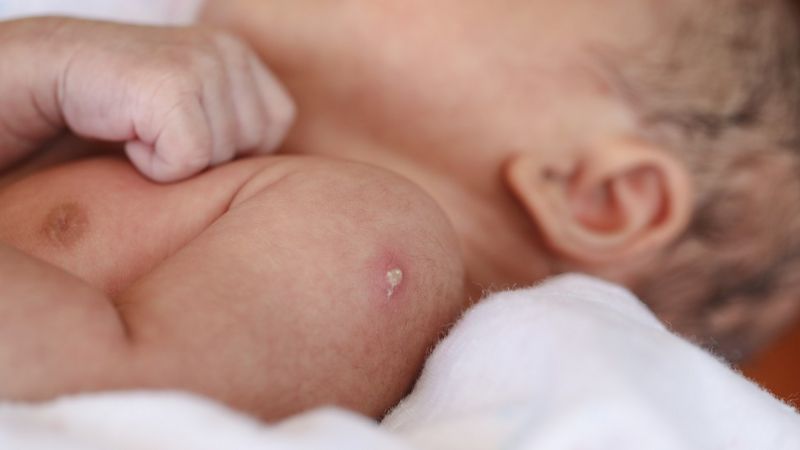
La mayoría de los vacunados con BCG experimentan una reacción en el lugar de la inyección que se considera normal y se denomina cicatriz de BCG.
El 18 de julio de 1921, un bebé recién nacido en París recibió la primera dosis de una vacuna pionera contra la tuberculosis.
Llegar a ese momento había llevado años de sacrificios a los dos científicos franceses que desarrollaron la vacuna, Albert Calmette y Camille Guérin.
Un siglo después, esa vacuna, llamada BCG (o Bacilo de Calmette-Guérin) es aún la única que existe contra la tuberculosis, una enfermedad que cada año mata en el mundo a más de 1,4 millones de personas.
Se estima que más de 100 millones de niños reciben la BCG cada año, y hasta la fecha más de 4 mil millones de dosis fueron administradas.
Pero la BCG es también «el mayor dolor de cabeza de la salud pública» según un experto, debido a las grandes variaciones en su eficacia que la ciencia no logra explicar cabalmente.
En el centenario de la célebre vacuna, recordamos su legado y su fascinante historia marcada por tragedias. Y exploramos por qué sigue la lucha sin cuartel de algunos científicos por una nueva vacuna contra la tuberculosis.
La tuberculosis y la BCG
La tuberculosis es una enfermedad infecciosa causada fundamentalmente por la bacteria Mycobacterium tuberculosis.
Otra especie de bacilo relacionada, Mycobacterium bovis, causa tuberculosis sobre todo en el ganado, pero también en humanos y en otros animales.
La tuberculosis ha causado más muertes que ninguna otra enfermedad infecciosa a lo largo de la historia y se estima que en los últimos dos siglos ha costado la vida a más de mil millones de personas.

La enfermedad suele afectar principalmente a los pulmones y se transmite de persona a persona por vía aérea.
«Cuando una persona con tuberculosis expulsa bacilos al toser, estornudar, hablar, entonces las personas que se encuentren cerca pueden inhalar estos bacilos e infectarse», le explicó a BBC Mundo la bioquímica Chyntia Carolina Díaz Acosta, doctora en biología molecular y celular e investigadora y docente en micobacterias en la Universidad Nacional de Asunción en Paraguay.
Uno de los grandes desafíos para combatir la TB es que la bacteria que la causa está presente en cerca de un cuarto de la población mundial, según la OMS. Y desde ese estado latente la infección puede volverse activa cuando se agudizan otros factores, como la pobreza y la desnutrición.
Qué es la tuberculosis latente que afecta a una de cada 4 personas
La vacunación con BCG se recomienda en menores de 1 año, idealmente en el recién nacido, en una dosis única que se administra por vía intradérmica (en el brazo), explicó Díaz Acosta.
«Cuando un niño vacunado entra en contacto con un paciente, lo que ocurre es que tendrá menor probabilidad de presentar formas graves de tuberculosis, al evitar la diseminación sanguínea de los bacilos que ingresaron a su organismo».
«Así, la vacuna BCG reduce la mortalidad infantil y mejora el sistema inmunitario ante la tuberculosis. No obstante, no consigue evitar la infección primaria ni la reactivación de la tuberculosis latente, que es la principal fuente de propagación de la micobacteria en la comunidad».
«La mayoría de los países con alta carga de morbilidad administran la vacuna BCG como parte de su programa nacional de inmunización pediátrica, pero en países donde la tuberculosis es poco frecuente, la estrategia preferida es la vacunación de grupos de alto riesgo».

Un hito histórico
La primera dosis de la BCG fue aplicada en el Hospital de la Charité en París, a un bebé cuya madre había muerto de tuberculosis poco después del parto.
La vacuna fue administrada por vía oral por dos pediatras, Benjamin Weill-Hallé, miembro del equipo de Calmette en el Instituto Pasteur, y Raymond Turpin.
Aquella primera dosis de la BCG «fue un hito que consagró una investigación iniciada en la década de 1890 por Calmette y Guérin, con el propósito de hallar una solución inmunológica contra la tuberculosis, quizás la enfermedad que generó mayores estragos en la salud pública a nivel mundial en aquel entonces», señaló a BBC Mundo Marcelo López Campillay (PhD), profesor de Historia de la Medicina en la Pontificia Universidad Católica de Chile.

En 1882, el científico alemán Robert Koch había descubierto el bacilo causante de la TB, desatando una carrera por desarrollar una vacuna contra la enfermedad.
En 1908, el médico Albert Calmette (1863-1933) y el veterinario Camille Guérin (1872-1961) comenzaron su trabajo en busca de una vacuna en el nuevo Instituto Pasteur en Lille.
Calmette había sido alumno del gran Louis Pasteur, uno de los fundadores de la bacteriología moderna, quien le había encargado abrir el primer Instituto Pasteur en una de las colonias de Francia (en Saigón, parte entonces de la Indochina Francesa).
Cuando en 1895 se estableció un Instituto Pasteur en Lille, fue a Calmette a quien se confió su dirección.
Un experimento de 13 años
En Lille, Calmette y Guérin comenzaron su búsqueda de una vacuna contra la TB trabajando a partir de la llamada «leche Nocard», una cepa virulenta de Mycobacterium bovis que Edmond Nocard, también alumno de Pasteur, había aislado de la ubre de una vaca tuberculosa.
La gran pregunta era cómo lograr un bacilo vivo pero no virulento y lo suficientemente atenuado como para generar una respuesta inmune sin causar la enfermedad.
A Calmette y Guérin les llevó más de una década atenuar el bacilo de Nocard.
«El trabajo de laboratorio que efectuaron Calmette y Guérin es un ejemplo de la paciencia y minuciosidad que caracterizan la vida de laboratorio, así como de cierto temple para superar adversidades sociales y políticas que enmarcan el desarrollo de la ciencia», afirmó López Campillay.

Los científicos cultivaron repetidamente al bacilo bovino en un medio con bilis de buey, glicerina y papa en sucesivos ciclos de atenuación.
Los cultivos «fueron ‘replicados’ cada 15 días en 230 ocasiones, tarea que involucró 13 años de trabajo que culminaron con la obtención de un bacilo atenuado que era inofensivo para todas las especies animales susceptibles a la tuberculosis».
«Este paciente trabajo tuvo que superar las inclemencias de la Primera Guerra Mundial, momento en el cual la ciudad de Lille tuvo que sufrir los fragores del combate», señaló el historiador.
«Se ha señalado que ese episodio demuestra el talante de Calmette, quien no cejó en su misión de aliviar el ‘dolor universal’ que significaba la tuberculosis, al punto que en esa etapa comenzó a escribir una de sus obras claves, ‘La infección bacilar y la tuberculosis’, la cual finalizó en 1920».
Durante la ocupación de Lille por tropas alemanas, Calmette y Guérin enfrentaron grandes dificultades para obtener las papas y bilis de buey necesarios para los cultivos del bacilo. El precio de las papas se había disparado, pero los científicos siguieron adelante con su experimento. Algunos relatos señalan que obtuvieron la bilis de buey de los propios veterinarios de las tropas alemanas.
El compromiso social de un «médico maestro»
Para López Campillay, Calmette fue «un médico que representó a una generación de profesionales que entendió que la medicina debía cumplir con un compromiso público».
El médico francés comprendió a la tuberculosis «como un problema social, porque él tuvo plena conciencia de que la peste blanca era una enfermedad de la marginalidad social».

Calmette también puede ser catalogado «como un fiel representante del médico-maestro».
«Uno de los investigadores que viajó a especializarse en Francia fue por ejemplo el médico y tisiólogo catalán Luis Sayé, que estudió en el laboratorio de Calmette y aprendió con él la técnica de vacunación de la BCG, la cual posteriormente difundió no solo en España, sino en Sudamérica a contar de la década de 1930».
Por su parte, Camille Guérin fue un veterinario y biólogo que se interesó tempranamente en las enfermedades infecciosas, «tal vez porque su padre murió por causa de la tuberculosis».
Su alianza profesional con Calmette es para López Campillay «un ejemplo de una labor interdisciplinaria que se transformó en una suerte de estándar en la educación superior del siglo XX».
La tragedia de Lübeck
Tras el éxito de las aplicaciones de la BCG en Francia, que para 1924 logró vacunar a 300 niños en forma segura, la vacuna comenzó a producirse a gran escala.
Pero este avance fue frenado por un episodio trágico.
El llamado desastre de Lübeck, ocurrido en 1930 en esa ciudad del norte de Alemania, puso momentáneamente en tela de juicio la expansión de la BCG. De un grupo de 250 niños inoculados, más de 70 murieron de tuberculosis.

Una investigación posterior determinó que las muertes no habían ocurrido por la vacuna. La causa de la tragedia fue que en los propios laboratorios de Lübeck, la vacuna había sido contaminada con una cepa virulenta del bacilo de TB.
La muerte de los niños afectó profundamente a Calmette, quien calificó la negligencia en Lübeck como una catástrofe.
«Fue un hecho que sacudió su compromiso social como médico, toda vez que él fue enfático en sostener que la difusión de la BCG por parte del Instituto Pasteur debía hacerse en forma gratuita y con fines estrictamente sanitarios dado que era un avance para la humanidad», señaló López Campillay.
La vacuna solo volvió a usarse ampliamente a nivel global tras el aumento de TB durante la Segunda Guerra Mundial.
En 1974, la OMS incorporó la BCG en su Programa Ampliado de Inmunización.
«El mayor dolor de cabeza»
A pesar de su amplio uso, la vacuna BCG ha sido descrita como «el mayor dolor de cabeza en salud pública» por Paul Fine, profesor de epidemiología de la Escuela de Higiene y Medicina Tropical de Londres.
«Cuando hablo del mayor dolor de cabeza me refiero a las cifras que muestran las diferencias en efectividad de la BCG en diferentes países y estudios», señaló Fine a BBC Mundo.
«Esto ha sido reconocido por más de 60 años y es aún debatido. Ha habido muchos estudios, tal vez unos 100, con resultados de efectividad de la vacuna que varían desde 0 a 80%. Esta estadística, conocida como eficacia de una vacuna, mide la proporción de personas inoculadas que son protegidas de una determinada enfermedad por una vacuna».

Díaz Acosta afirmó que «el nivel de eficacia protectora de la BCG continúa siendo controvertido, aunque sea la más antigua de las vacunas utilizadas actualmente».
Algunos reportes por meta-análisis lograron estimar que la vacuna BCG previene en los niños «aproximadamente el 73% de la meningitis tuberculosa (cuando el bacilo de TB afecta las meninges o membranas que recubren el cerebro y la médula espinal) y el 77% de la tuberculosis miliar (la tuberculosis diseminada por el cuerpo a través de la corriente sanguínea) desde el nacimiento hasta los 5 años de edad».
Pero su eficacia contra la tuberculosis pulmonar pediátrica «ha variado desde ninguna protección hasta una protección muy alta (0 a 80%)».
Aun con todas estas consideraciones, «existe el consenso de que la BCG es claramente protectora en el niño y que además por su bajo costo debe seguir desempeñando un importante papel en los Programas de Control de la Tuberculosis».
¿A qué se deben las diferencias en eficacia?
Se han propuesto diferentes explicaciones, incluyendo diferencias en el diseño de los estudios o en las vacunas.
Y es que no existe una única vacuna BCG.
«Actualmente existen diversas cepas de vacunas BCG, conocidas por el nombre del lugar de producción, como la cepa francesa Pasteur 1173 p2, la danesa 1331, la Glaxo 1077, la Tokio 172-1…la BCG Paris, que son utilizadas a nivel mundial. En términos de eficacia, ninguna cepa de BCG se ha descrito como la mejor», afirmó Díaz Acosta.

Para Díaz Acosta, investigadora y docente de la Universidad Nacional de Asunción, la explicación más plausible de las diferencias en eficacia se basa en las distintas exposiciones a micobacterias ambientales.
Fine señala que «probablemente la explicación más aceptada para la heterogeneidad en efectividad tiene que ver con la exposición a diferentes micobacterias en el agua y el suelo en diferentes regiones, que pueden bloquear el efecto de la BCG hasta cierto punto».
Algo que favorece esta explicación es la observación de que la efectividad de la BCG es generalmente mayor en regiones templadas en latitudes altas que en regiones tropicales de latitudes bajas. Y las micobacterias en el ambiente son más prevalentes en los climas más cálidos.
Díaz Acosta coincide con Fine en que la explicación más plausible se basa en las diferentes exposiciones a micobacterias ambientales de las personas que viven en climas cálidos y las que viven en climas fríos.
Esa exposición podría afectar la respuesta inmunitaria inducida por la vacuna o impactar en la medición de la eficacia.
Otros usos de la BCG
La vacuna BCG también actúa contra otras enfermedades más allá de la TB, según estudios.
«La vacuna BCG parece ser más efectiva contra la lepra que contra la tuberculosis y su amplio uso es probablemente una de las razones de la caída en los casos de lepra», explicó Fine.
«Y hay evidencia de que podría tener un efecto no específico de estimular la respuesta del sistema inmune contra una variedad de infecciones. Cuánto dura esa respuesta y cuán efectiva es contra diferentes patógenos es algo que se desconoce».
El misterio de por qué algunas vacunas proporcionan extraordinarios beneficios más allá de los esperados
«También se ha afirmado que podría proteger contra la covid, pero la evidencia no es consistente. Hay ahora varias vacunas específicas contra la covid que son mucho más efectivas que la BCG en la protección contra esta enfermedad».

La BCG es utilizada además en el tratamiento del cáncer superficial de vejiga, según le explicó a BBC Mundo el Dr. José Luis Álvarez Ossorio, vocal de Actividades Científicas de la Asociación Española de Urología.
«La vejiga se divide en tres capas microscópicas, siendo la última capa o capa más profunda la que se denomina capa muscular. La BCG se utiliza para aquellos tumores que afectan a las dos primeras capas».
El uso de la BCG es considerado en este caso «como un tratamiento de inmunoterapia», afirmó el urólogo.
«Se administra directamente en la vejiga de forma líquida; es decir, mediante instilaciones. Dicha instilación provoca que se activen las células del sistema inmunitario en la vejiga para que ataquen a las células cancerosas de la vejiga».
«En aquellos pacientes en los que la BCG funciona puede llegar a ser un tratamiento curativo, reduciendo las muertes por cáncer de vejiga».
La lucha por una nueva vacuna
«La tuberculosis mata cada año casi un millón y medio de personas a pesar de que la actual vacuna BCG es de las más utilizadas del mundo, y esto es porque no protege contra las formas pulmonares de TB en adolescentes y adultos. Es por eso que es muy urgente encontrar una nueva vacuna contra estas formas de la enfermedad», le explicó a BBC Mundo Carlos Martín, catedrático de microbiología en la Facultad de Medicina de la Universidad de Zaragoza.
El profesor Martín fue quien diseñó una de las vacunas candidatas consideradas más prometedoras contra la TB, la vacuna denominada Mtbvac, que es diferente a la BCG.
«Mtbvac es una vacuna viva atenuada como BCG, pero partimos de una cepa clínica de Mycobacterium tuberculosis (que causa La tuberculosis en humanos), mientras en la BCG se partió de una cepa de Mycobacterium bovis (causante de TB en animales)».

El desarrollo de la vacuna se realizó en la Universidad de Zaragoza en colaboración con el Instituto Pasteur de París, y la atenuación de Mtbvac se consiguió eliminando genes importantes en la virulencia del bacilo de la TB, señaló el científico.
«Mtbvac está diseñada para proteger contra las formas respiratorias de TB y si protege, mejor reemplazar a la BCG».
«La vacuna candidata está finalizando la Fase 2 en bebés y la Fase 2 en adultos infectados y no infectados de tuberculosis para estudiar la seguridad e inmunogenicidad de Mtbvac en Sudáfrica y definir la dosis para la Fase 3 de eficacia en bebés que comenzará a principios de 2022».
Desarrollar una nueva vacuna contra la tuberculosis ha sido un enorme desafío.
Al igual que en el caso de otras enfermedades para las que se están buscando vacunas como la malaria y el sida, se trata de «enfermedades todas ellas de la pobreza en las que las grandes compañías farmacéuticas no muestran el mismo interés que para las vacunas contra la covid-19, por lo que la financiación es en muchos casos pública y no suficiente para acelerar el desarrollo clínico», afirmó Martín.
«Los esfuerzos de nuestros antepasados»
Son muchas las lecciones que pueden extraerse de la historia de la BCG, como el papel crucial de las instituciones científicas como el Instituto Pasteur, según López Campillay.
Para el profesor de historia de la medicina, existen dos reflexiones fundamentales a propósito del centenario de la vacuna.
Una de ellas es la importancia de la alianza entre política y ciencia como un pilar del bienestar social.
«Tal como fue fundamental el trabajo que desarrollaron pacientemente Calmette y Guerin por más de una década, no se debe desmerecer el respaldo de las instituciones públicas que ampararon la difusión de una nueva vacuna mediante campañas de inmunización, que tras la Segunda Guerra Mundial alcanzaron dimensiones globales con el apoyo que la OMS y la Unesco brindaron a la BCG».

En segundo lugar, según el historiador, desde su origen la vacuna de Calmette y Guérin contó con una aplicación universal y gratuita, que afianzó el derecho a la salud como parte del ejercicio de la ciudadanía.
Ante el reto de la tuberculosis, que dejó en evidencia graves desigualdades sociales, la BCG emergió como una herramienta de equidad social, según López Campillay.
Y de la misma forma «la covid-19 ha revelado que las epidemias infecciosas siguen siendo parte de nuestro mundo y que las inequidades sociales acentúan sus efectos en forma dramática».
Para el historiador de la ciencia, «un siglo después de la primera aplicación de la BCG, las sociedades del siglo XXI deben tomar conciencia de una historia de la salud donde es posible apreciar la complejidad de los esfuerzos que realizaron nuestros antepasados para enfrentar grandes desafíos sanitarios».
«Ellos nos legaron conocimientos científicos y políticas sanitarias, como muy bien lo representa la BCG, que en el año 2021 han sido determinantes en las campañas de inmunización para superar la urgencia que ha significado la pandemia de coronavirus».
Fuente: BBC




